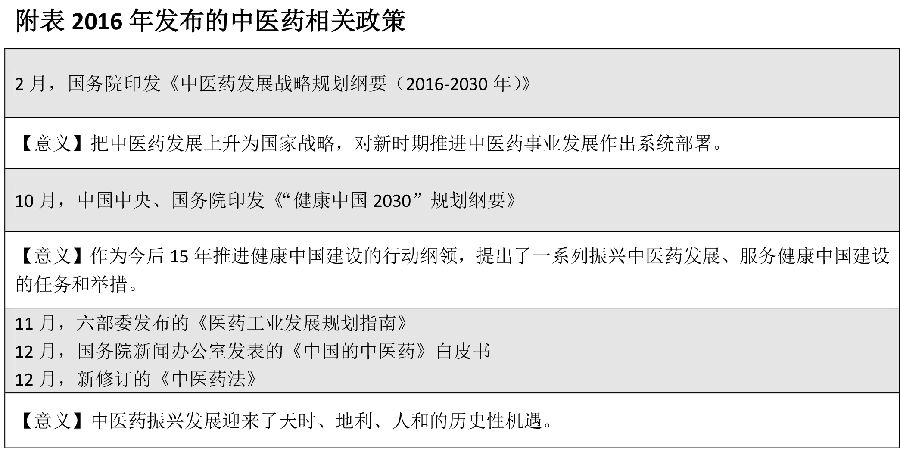
从10月发布《“健康中国2030”规划纲要》,到11月发布《医药工业发展规划指南》、《中国的中医药》白皮书,再到刚刚发布的《中医药法》,有关中医药相关政策在2016年的第四季度密集发布。相关政策显示出中医药在经济社会发展中的地位和作用愈加重要,中医药行业发展已然迎来了新的历史高峰点。
国家制定的2020年中医药目标为实现人人基本享有中医药服务;2030年目标为中医药服务领域实现全覆盖,并推动中医药服务全世界。以上两个目标非常宏伟,这是基于:“十二五”期间中药创新能力显著提升,中药全过程质量控制水平提高;屠呦呦获得诺贝尔奖意味着我国中医药创新获得国际进一步认可;此外,面对医保日益加重的支付压力,中医药价格优势也是国家大力发展中医药的原因。
在这样的大好背景下,笔者从中药创新、中药材(饮片)和中药国际化三个方面,分析未来中药行业中的立项机会。笔者认为,一切规划都是为了中药大品牌和国际化。
【中药创新】
何为现代中药的立项方向?
“坚持继承与创新”是中医药发展必须要学习的课题,国家一直鼓励运用现代科学技术研究开发传统中成药,这意味着中成药的开发需要既保持特色优势又要积极利用现代科学技术。而具体到立项上,什么才是既“继承”又“创新”的项目?
在“中药创新”项目中,国家剑指在中医优势病种如心脑血管疾病、自身免疫性疾病、妇儿科疾病、消化科疾病领域,挖掘经典名方,开展复方、有效部位及有效成分中药重点品种研究,发展质量稳定可控、临床优势突出的现代中药。《医药工业发展规划指南》更提出了要建设和整合中药化学成分库,这意味着国家认可中药的创新是往天然药物化学方向研究,中药成分规模化高效分离与制备技术作为重点发展目标更是印证了这一点。
值得注意的是,通过中药再评价发掘新适应症也是创新手段的一种:针对已上市品种,运用现代科学技术,开展药品上市后疗效、安全、制剂工艺和质量控制再评价,深挖临床价值,明确优势治疗领域,开发新的适应症。
适应症挖掘方面,“防治”是中药新药和已上市药品共同关注的重点方向,其中包括但不限于与化学药一同联合攻关防治重大疑难疾病、重大传染病;以及中药对常见病、多发病、慢性病的防治,这一切正好是“十二五”期间中医药获得良好效果对应的疾病领域。
来源于古代经典名方的中药复方制剂的二次开发也值得关注。根据新《中医药法》,古代经典名方是指至今仍广泛应用、疗效确切、具有明显特色与优势的古代中医典籍所记载的方剂。这类方剂在申请药品批准文号时,可以仅提供非临床安全性研究资料,但是具体目录由国务院中医药主管部门会同药品监督管理部门制定,预计目录在短期内不会大范围放开。此类复方制剂从口服改为外用是否可以免临床将是企业所关注的,免临床且适用于儿科的复方制剂将会是企业追捧的热点。
制剂产业化创新方面,国家扶持符合中药特点的缓控释、经皮和粘膜给药、物理改性和掩味等新型制剂技术。其中,缓控释技术更适合于心脑血管疾病、消化科疾病用药的开发,经皮和粘膜给药则适合自身免疫性疾病、妇儿科疾病用药的开发,掩味则更针对中药儿科制剂的开发。中药制剂物理改性是指采用喷雾干燥、流化床、机械磨压、粉末沉积等物理机械方法对中药制剂原料的表面进行修饰加工,改变中药制剂原料的不良物理性质,以便中药制剂的安全性、有效性和稳定性得以提高,中药制剂物理改性主要针对中药提取物为制剂原料的中药制剂的开发。
回顾 “十二五”中医药制剂成果。
2015年,中药工业总产值7866亿元,占医药产业规模的28.55%,成为新的经济增长点。全国国产中药民族药约有6万个药品批准文号,由2088家通过药品生产质量管理规范(GMP)认证的制药企业生产中成药,包括丸、散、膏、丹等传统剂型和滴丸、片剂、膜剂、胶囊等40多种剂型。“十二五期间”,我国基本建立了以药材生产为基础、工业为主体、商业为纽带的现代中药产业体系。
中医药主要贡献的领域在常见病、多发病、疑难杂症的防治,在重大疫情防治和突发公共事件医疗救治中也发挥重要作用,如治疗传染性非典型肺炎的疗效得到世界卫生组织肯定。中医治疗甲型H1N1流感的优良成果引起国际关注。同时,中医药在防治艾滋病、手足口病、人感染H7N9禽流感等传染病,以及四川汶川特大地震、甘肃舟曲特大泥石流等突发公共事件医疗救治中,都发挥了独特作用。因将传统中药的砷剂与西药结合治疗急性早幼粒细胞白血病的疗效明显提高,王振义、陈竺获得第七届圣捷尔吉癌症研究创新成就奖。
【中药材和中药饮片】
质量可控依然是主命题。
“十三五”规划依然老生常谈地从中药材和中药饮片的质量管控这个基础源头出发,以提升中药质量水平:提升大宗道地药材标准化生产和产地加工技术,建设中药材全过程追溯体系,完善中药质量标准体系,从而提升中药全产业链质量控制水平,最终达到提高中药产品质量均一性和可控性的目标。
中药材资源可持续利用计划仍是规划重点。开展全国中药资源普查,建立中药资源动态监测和技术服务网络,建立中药种质资源保护体系,保护药用种质资源及生物多样性。
虽然国家不再要求GAP生产认证,但从可持续发展角度,若企业的主营中药产品的有效部位不能通过合成获取,企业应战略性布局建设中药材规范化道地种植养殖基地,特别是道地中药材品种选育,积极建立地理标志产品品牌。
此外,2015年版药典已经提高了农药残留物的检测鉴定标准,并加大了行业链的检查成本。新《中医药法》提出禁止在中药材种植过程中使用剧毒、高毒农药。这意味对农药、肥料的管控预计未来还会更严格。企业关键药材布局道地种植养殖基地,将能更好地管理药材。
针对濒危稀缺药材,发展人工繁育技术,特别是推动麝香、沉香、冬虫夏草等产品野生变种植养殖。对于短缺中药材,国家甚至鼓励企业在境外收购或投资建设生产基地,充分利用境外环境资源,这意味着中药企业可能会加大在东南亚和非洲等生态环境较为良好且投资成本较低的领域开发中药种植业。
除了中药饮片和中药基本药物,中药注射剂的质量提升,中药大品种的生产质量控制标准和产品标准制定和提升也是产品质量升级工程计划中的项目。
回顾“十二五”中药资源普查成果。
目前我国中药资源普查已初步建成由1个中心平台、28个省级中心、65个监测站组成的中药资源动态监测信息和技术服务体系,以及16个中药材种子种苗繁育基地和2个种质资源库。
【中药国际化】
质量提升与中药大品牌。
中药想要借助“一带一路”政策走出国门,关键还是要解决药品安全问题,主要在质量标准、有效性、安全性等方面。中药创新和中药质量提升都是为了中药国际标准的制定,从而打造优质中药品牌,鼓励中药国际注册,引领中药企业走出去,期望在“十三五”期间有更多中药在发达国家市场上市。
在医保支付能力已接近饱和的背景下,化学药新药开发要求临床疗效优效对企业而言压力较大,化学仿制药将面临价格战竞争惨烈,从中药有效化学成分中挖掘“防治”方向研发新药未尝不是一个方向。
不过,天然药化研发方向至少还需要10~15年铺垫,在短期内可能较难看到中药大范围爆发成果。实际上,我国产学研项目不缺天然药化的临床前项目,但由于靶点、机理等研究不够深入,致使企业不敢贸然投入,归根到底是企业缺乏项目评估的领军人才。中医药企业想成就中药大品牌和国际化,科学家引导产品研发规划型企业更有可能成功。
回顾“十二五”中药国际化成果。
按《中国的中医药》白皮书,中医药已传播到183个国家和地区。其中,中药逐步进入国际医药体系,已在俄罗斯、古巴、越南、新加坡和阿联酋等国以药品形式注册。中国医保商会等多方努力之下,截至2016年5月,已有包括人参、陈皮、白术、大黄、水红花子、虎杖、三七等66种中药材进入欧洲药典。
国内已有先驱者为中药在欧美国际主流医药市场上市作努力。
兰州佛慈于2011年将浓缩当归丸欧盟传统草药简化注册ECTD申请材料正式提交瑞典国家药品管理局,成为国内第一种在欧盟申请注册的中成药。
成都生物研究所和成都地奥制药研制生产的“地奥心血康胶囊”2012年获准欧盟注册上市,是我国自主知识产权治疗性药品首次进入发达国家市场。
天士力复方丹参滴丸Ⅲ临床试验项目在美国、加拿大、俄罗斯、乌克兰、格鲁吉亚、白俄罗斯、墨西哥、巴西及中国台湾9个国家和地区127个临床中心顺利进行;丹参胶囊顺利获欧盟植物药品注册批件。
(选自《医药经济报》)